Capnografía volumétrica
La medición de la señal de CO₂ a tiempo es muy útil para la detección de diversas afecciones, tanto durante la anestesia como fuera del quirófano (especialmente en la unidad de cuidados intensivos). Entre las aplicaciones más frecuentes se encuentran la confirmación de la intubación endotraqueal, la monitorización de la ventilación alveolar durante la cirugía y la detección temprana de la posibilidad de desconexión del paciente del ventilador. En los últimos años se han desarrollado diversas aplicaciones nuevas: la monitorización de la hipoventilación durante la sedación en ventilación espontánea, la evaluación de la mecánica respiratoria (VM), la evaluación de la eficacia de la reanimación cardiopulmonar, la asistencia durante el proceso de traqueostomía percutánea, la confirmación de la respuesta del sistema nervioso durante la apnea e incluso la reducción de costes e intervenciones asociadas al análisis de gases sanguíneos y la tasa metabólica.
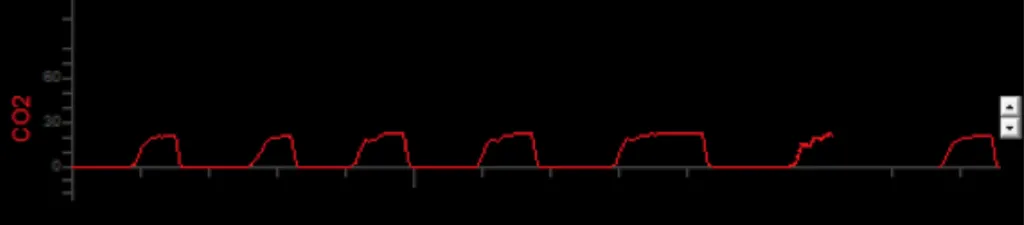
Al sincronizar la señal de volumen con la señal de CO2, se puede obtener información mucho más completa. Al combinar el gráfico paramétrico de CO2 con el volumen exhalado, se construye el gráfico de capnografía volumétrica.
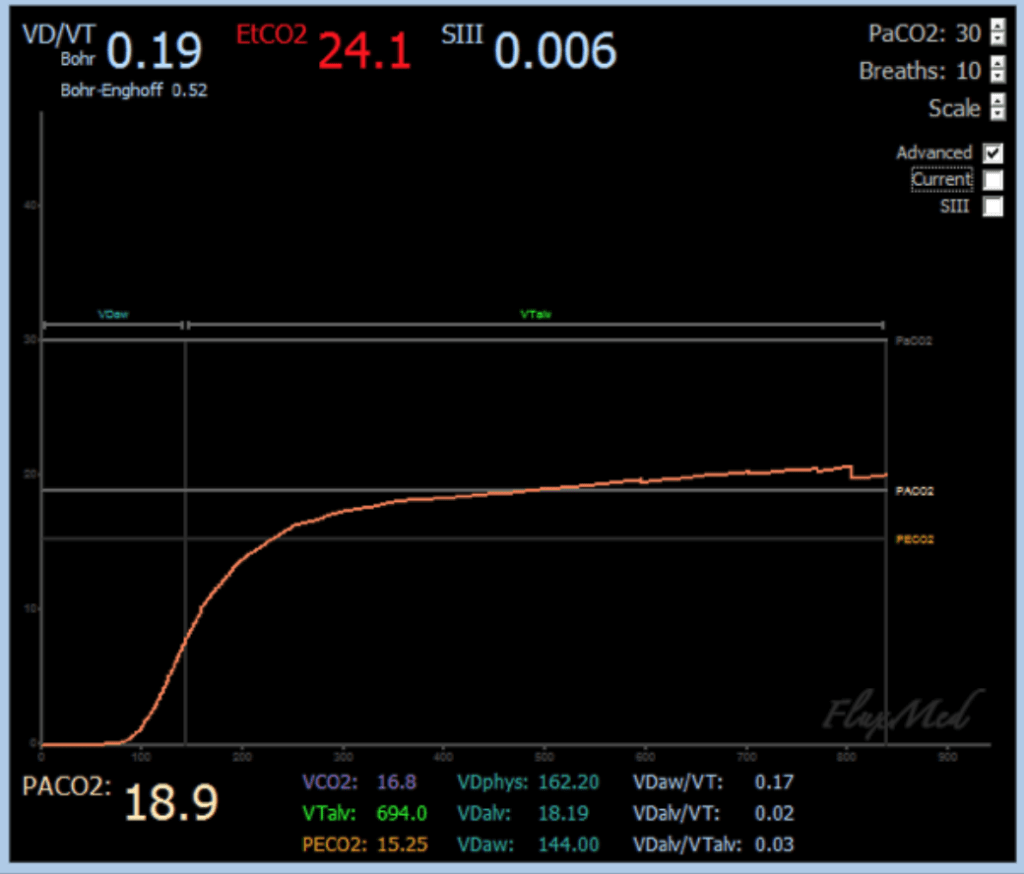
Desde un punto de vista clínico, se puede obtener información muy valiosa, ya que permite calcular el espacio muerto alveolar y el gasto cardíaco. La monitorización del espacio muerto alveolar puede ser muy útil para evaluar la respuesta a las maniobras de reclutamiento y la fisiopatología de la enfermedad del paciente (especialmente en el SDRA y en el diagnóstico de tromboembolia pulmonar).
La monitorización del espacio muerto, con diferentes configuraciones del respirador, permite comprender mejor la ventilación, la perfusión y las características metabólicas del paciente. La producción de CO2 (VCO2) es el área bajo la curva. La fracción espirada de CO2 (PECO2) es el valor espirado promedio. Un nuevo algoritmo permite calcular la concentración alveolar de CO2 (PACO2). Mediante la ecuación de Bohr, se puede calcular el espacio muerto fisiológico (Vd/Vt) y sus componentes. Todo esto se realiza respiración a respiración y de forma no invasiva.
Si se toma una muestra de gases arteriales del paciente para medir la concentración arterial de CO2 (PaCO2), mediante la ecuación de Bohr-Enghoff, se puede estimar el shunt del paciente. El software FluxView calcula automáticamente todos los siguientes parámetros a través de una interfaz de usuario fácil y amigable.
| Parámetros | Descripción |
|---|---|
| Vd/Vt. Bohr | Relación entre el espacio muerto fisiológico y el volumen corriente calculada con la ecuación de Bohr |
| VD/Vt Bohr-Enghoff | Relación entre el espacio muerto fisiológico y el volumen corriente calculada con la ecuación de Bohr |
| EtCO2 | Concentración de CO2 al final de la espiración |
| SIII | Fase III de la pendiente |
| PaCO2 | Presión parcial de CO2 alveolar |
| VCO2 | Volumen de CO2 producido por la respiración |
| V12 | Volumen de corriente alveolar |
| PECO2 | Fracción de CO2 expirada |
| VDfísico | Espacio muerto fisiológico |
| VDalv | Espacio muerto alveolar |
| VDaw | Espacio muerto de la vía aérea |
| VDaw/VT | Relación entre el espacio muerto de la vía aérea y el volumen corriente |
| VDalv/VT | Relación entre el espacio muerto alveolar y el volumen corriente |
| VDalv/VTalv | Relación entre el espacio muerto alveolar y el volumen corriente alveolar |


